ViiV, tập đoàn sở hữu bản quyền thuốc tiêm tác dụng kéo dài Cab, đồng ý chia sẻ bản quyền cho một số nhà sản xuất thuốc generic để cung cấp thuốc giá hợp lý cho các nước đang phát triển.
ViiV, tập đoàn sở hữu bản quyền thuốc tiêm tác dụng kéo dài Cab, đồng ý chia sẻ bản quyền cho một số nhà sản xuất thuốc generic để cung cấp thuốc giá hợp lý cho các nước đang phát triển.
Theo một thỏa thuận mới, các nhà sản xuất được cấp phép sẽ có thể cung cấp các phiên bản chung của thuốc điều trị dự phòng trước phơi nhiễm HIV (PrEP) cabotegravir tác dụng kéo dài của ViiV cho các quốc gia đang phát triển.
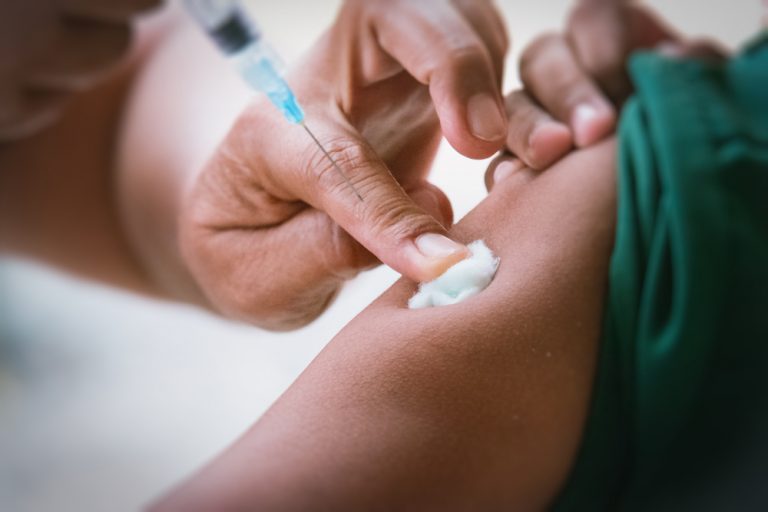
Bác sĩ tiêm cho một bệnh nhân ở cánh tay trên bằng ống tiêm
ViiV Healthcare và Tổ chức Bằng sáng chế Thuốc (MPP) đã ký một thỏa thuận cấp phép tự nguyện mới để tăng khả năng tiếp cận với cabotegravir tác dụng dài (LA) để điều trị dự phòng trước phơi nhiễm với HIV (PrEP) ở những người kém phát triển, có thu nhập thấp, thu nhập trung bình thấp và Các nước châu Phi cận Sahara.
Thông qua thỏa thuận này, các nhà sản xuất chung được chọn sẽ có cơ hội phát triển, sản xuất và cung cấp các phiên bản chung của cabotegravir LA cho PrEP ở 90 quốc gia, tùy thuộc vào các phê duyệt quy định bắt buộc. Dự kiến, thỏa thuận này sẽ giúp cho phép tiếp cận trên quy mô lớn đối với cabotegravir LA chung cho PrEP.
Thông báo này được đưa ra cùng ngày với việc ViiV công bố dữ liệu mới từ thử nghiệm 084 của Mạng lưới Thử nghiệm Phòng chống HIV (HPTN) đánh giá cabotegravir LA cho PrEP ở phụ nữ ở châu Phi cận Sahara. Nghiên cứu này cho thấy cabotegravir LA tiếp tục chứng minh hiệu quả vượt trội trong việc ngăn ngừa nhiễm HIV mới ở phụ nữ khi so sánh với viên nén emtricitabine / tenofovir disoproxil fumarate (FTC / TDF) uống hàng ngày, với tỷ lệ nhiễm HIV thấp hơn 89%. Công ty cũng công bố dữ liệu an toàn khi mang thai mới, không có dị tật bẩm sinh được báo cáo trong 43 trường hợp mang thai xảy ra ở các bà mẹ sử dụng cabotegravir, khi những người tham gia ngừng tiêm cabotegravir cho đến khi ngừng cho con bú.
Mỗi năm, có khoảng 1,5 triệu trường hợp nhiễm HIV mới trên toàn thế giới, hầu hết xảy ra ở các quốc gia hạn chế về nguồn lực, với phụ nữ và trẻ em gái vị thành niên bị ảnh hưởng không tương xứng. Mặc dù các lựa chọn PrEP bằng đường uống có sẵn ở nhiều quốc gia, những thách thức về tuân thủ và kỳ thị đã hạn chế tác động của chúng ở một số người dân. MMP cho biết trong một tuyên bố tiếp cận một phương án phòng chống HIV hiệu quả có thể góp phần đáng kể vào mục tiêu chấm dứt đại dịch.
Giấy phép tự nguyện mới được công bố được xây dựng dựa trên quan hệ đối tác lâu dài giữa ViiV Healthcare và MPP, đã rất thành công trong việc tạo điều kiện thuận lợi cho việc sản xuất và bán các phiên bản chung của thuốc ViiV Healthcare dạng uống ở các quốc gia bị ảnh hưởng nhiều nhất bởi HIV và ít có khả năng chi trả cho việc điều trị và quan tâm, MMP nói thêm. Đặc biệt, việc cấp phép tự nguyện đã cho phép tiếp cận các sản phẩm gốc có chứa một loại thuốc cải tiến khác của ViiV Healthcare, dolutegravir, cho ít nhất 20 triệu người nhiễm HIV ở các quốc gia có thu nhập thấp và trung bình, kể từ tháng 12 năm 2021.
Deborah Waterhouse, Giám đốc điều hành của ViiV Healthcare nhận xét: “Thông báo của ngày hôm nay thể hiện một thời điểm có khả năng thay đổi cuộc chơi trong công tác phòng chống HIV. Cho phép tiếp cận trên quy mô lớn với cabotegravir LA chung cho PrEP có thể đóng một vai trò quan trọng trong việc ngăn chặn lây truyền HIV, đặc biệt là ở phụ nữ và trẻ em gái vị thành niên, và giúp chấm dứt đại dịch HIV. Tôi tự hào rằng thông qua quan hệ đối tác lâu dài với MPP, chúng tôi tiếp tục đóng vai trò của mình trong việc mở rộng khả năng tiếp cận của người dân ở các quốc gia hạn chế về tài nguyên đối với các loại thuốc cải tiến mới ”.
Giấy phép tự nguyện này là một phần của phương pháp tiếp cận toàn diện để cho phép tiếp cận trên quy mô lớn đối với cabotegravir LA cho PrEP ở các nước Châu Phi kém phát triển, có thu nhập thấp, thu nhập trung bình thấp và cận Sahara.
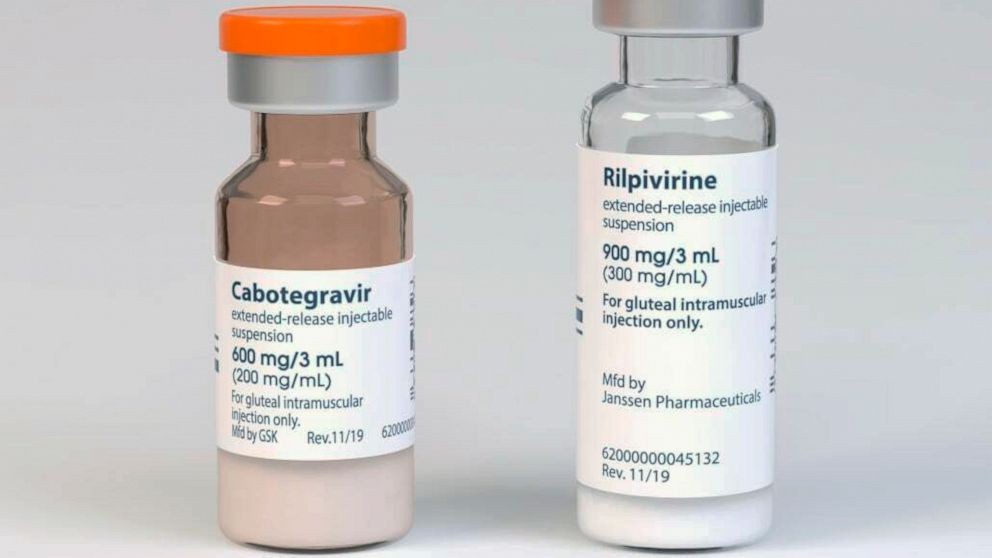
Do sự phức tạp của cabotegravir LA, so với các lựa chọn PrEP đường uống, bao gồm cả việc khó sản xuất hơn, ViiV Healthcare và MPP sẽ hợp tác chặt chẽ với các bên liên quan và các nhà sản xuất chung được lựa chọn thông qua quy trình thể hiện sự quan tâm của MPP để cho phép tiếp cận với cabotegravir LA chung cho PrEP càng sớm càng tốt.
Cabotegravir LA cho PrEP là một loại thuốc tiêm có tác dụng kéo dài, cho đến nay, mới chỉ được chấp thuận theo quy định để sử dụng trong phòng chống HIV ở Hoa Kỳ (dưới tên thương hiệu Apretude). Người lớn và thanh thiếu niên có nguy cơ nặng ít nhất 35kg được phép sử dụng PrEP để giảm nguy cơ lây nhiễm HIV-1 qua đường tình dục. Các cá nhân phải có xét nghiệm HIV-1 âm tính trước khi nhận.